貫壁性(Epi-M-Endo 細胞)再分極時間の不均一性(内因性)
遺伝子異常(
QT 延長
貫壁性再分極時間
(不応期)の不均一性↑
QT 延長
貫壁性再分極時間
(不応期)の不均一性
再分極電流↓
各細胞群APD
の均一な延長
M 細胞APD の
選択的延長
EAD からの異常自動能
(期外収縮)
β受容体刺激
torsade de pointes(リエントリー)
LQT1,(5, 11) LQT2,3(, 6),(9,10,12,13) LQT1-13
(IKs↓,IKr↓,IKl↓,IKACh↓, late INa↑,ICa↑)
KCNJ2,CACNA1C,CAV3,SCN4B, AKAP-9, SNTA1, KCNJ5
KCNQ1,KCNH2,SCN5A,ANKB, KCNE1,KCNE2,
遺伝子異常(
QT 延長
貫壁性再分極時間
(不応期)の不均一性↑
QT 延長
貫壁性再分極時間
(不応期)の不均一性
再分極電流↓
各細胞群APD
の均一な延長
M 細胞APD の
選択的延長
EAD からの異常自動能
(期外収縮)
β受容体刺激
torsade de pointes(リエントリー)
LQT1,(5, 11) LQT2,3(, 6),(9,10,12,13) LQT1-13
(IKs↓,IKr↓,IKl↓,IKACh↓, late INa↑,ICa↑)
KCNJ2,CACNA1C,CAV3,SCN4B, AKAP-9, SNTA1, KCNJ5
KCNQ1,KCNH2,SCN5A,ANKB, KCNE1,KCNE2,
2. QT延長症候群の発生機序
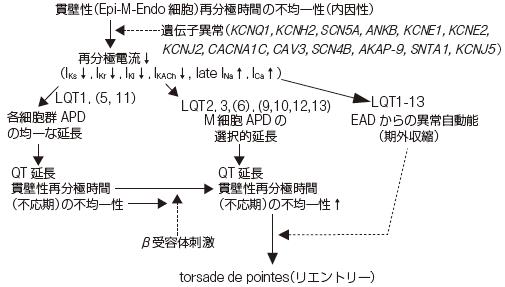
図1 先天性QT 延長症候群のQT 延長とTdP 発生機序
II. 総論 >
2. QT延長症候群の発生機序
先天性QT 延長症候群のRomano-Ward 症候群では,現在までに8 つの染色体上に13 個の遺伝子型が報告されている.いずれの遺伝子型でも,外向きK+ 電流
が減少(LQT1,2,5,6,7,11,13),内向きNa+ 電流が増加(LQT3,9,10,12),または内向きCa2+ 電流が増加(LQT4,8) することにより活動電位持続時間
(action potential duration:APD)が延長し,共通の表現型である心電図上のQT 延長を呈する.
単相性活動電位(monophasic action potential:MAP)記録を用いた臨床研究により,QT 時間の延長はMAP 持続時間(MAPD)の延長によることが証明された.
また,イソプロテレノールやエピネフリンなどのカテコラミン点滴静注により早期後脱分極(early afterdepolarization:EAD)様のhump が記録され,TdP 第1 拍目の心
室期外収縮の機序として,EAD からの撃発活動の関与することが直接的に証明されている.
一方,カテコラミン投与により心室筋各部位のMAPDの不均一性(spacial dispersion of repolarization:SDR)も増大し,TdPの維持にはSDRの増大によるリエント
リーも重要と考えられる.その後,動脈灌流左室心筋切片を用いた薬理学的QT 延長症候群モデルにより,先天性QT 延長症候群患者におけるTdP の細胞学的成因
がさらに明らかとなった.LQT1,LQT2,LQT3 の各モデルでは,しばしば心室期外収縮(単発または連発)の2 段脈に引き続いてTdP が誘発される.自然発生のTdP
を認めない場合でも, APD が最短の心外膜(Epi)細胞からの単発期外刺激により容易にTdP が誘発される.一方,TdP の引き金となる心室期外収縮は,比較的
QRS 幅が狭く,心内膜側心筋細胞側からのペーシング波形と同じ極性を示すことから,mid-myocardial(M)細胞または心内膜(Endo)側のPurkinje 細胞を起源とす
るEAD からの撃発活動が機序と考えられる場合もある.いずれのQT 延長症候群モデルでも,M細胞のAPD の相対的な延長によりtransmural dispersion of
repolarization(TDR)が増大しており,TdPの2 発目以降の機序には,心室筋各部位のSDR の増大に加えて,貫壁性のTDR の増大を基質とするリエントリーも重要
であると考えられる.図1 に臨床的および実験的検討から考えられる先天性QT 延長症候群のQT 延長およびTdP の発生機序を示す.

【ダイジェスト版】
QT延長症候群(先天性・二次性)とBrugada症候群の診療に関する
ガイドライン(2012年改訂版)
Guidelines for Diagnosis and Management of Patients with Long QT Syndrome and
Brugada Syndrome( JCS 2012)
ガイドライン(2012年改訂版)
Guidelines for Diagnosis and Management of Patients with Long QT Syndrome and
Brugada Syndrome( JCS 2012)
